|
Avertissement
|
||
|
Si vous arrivez
directement sur cette page, sachez que ce travail est
un rapport d'étudiants et doit être pris
comme tel. Il peut donc comporter des imperfections ou
des imprécisions que le lecteur doit admettre
et donc supporter. Il a été
réalisé pendant la période de
formation et constitue avant-tout un travail de
compilation bibliographique, d'initiation et d'analyse
sur des thématiques associées aux
technologies biomédicales. Nous ne faisons aucun usage
commercial et la duplication est libre. Si vous
avez des raisons de contester ce droit d'usage,
merci de nous
en faire part . L'objectif de la
présentation sur le Web est de permettre
l'accès à l'information et d'augmenter
ainsi les échanges professionnels. En cas
d'usage du document, n'oubliez pas de le citer comme
source bibliographique. Bonne lecture...
|
||
|
|
||
 |
 |
|
|
Référence
à rappeler : Introduction de la norme NF
EN 62353 au Centre Hospitalier de Boulogne sur Mer,
Olivier Legrand, Stage, Certification Professionnelle
ABIH, UTC, 2012
URL : http://www.utc.fr/abih ; Université de Technologie de Compiègne |
||
|
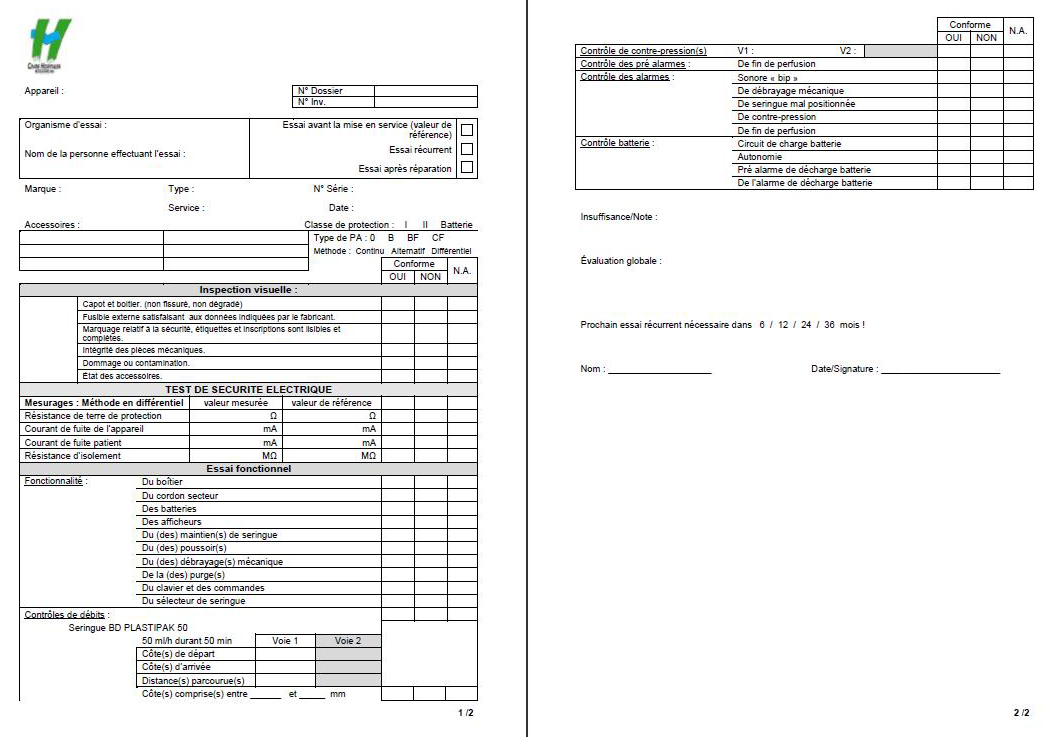
Ce rapport a
été réalisé dans le contexte
de la sécurité des patients et du
personnel, en introduisant la nouvelle norme
internationale sur les essais des appareils
électromédicaux : la CEI 62353 de 2007. Dans ce rapport, vous
trouverez des explications sur les
spécificités de la norme et proposition
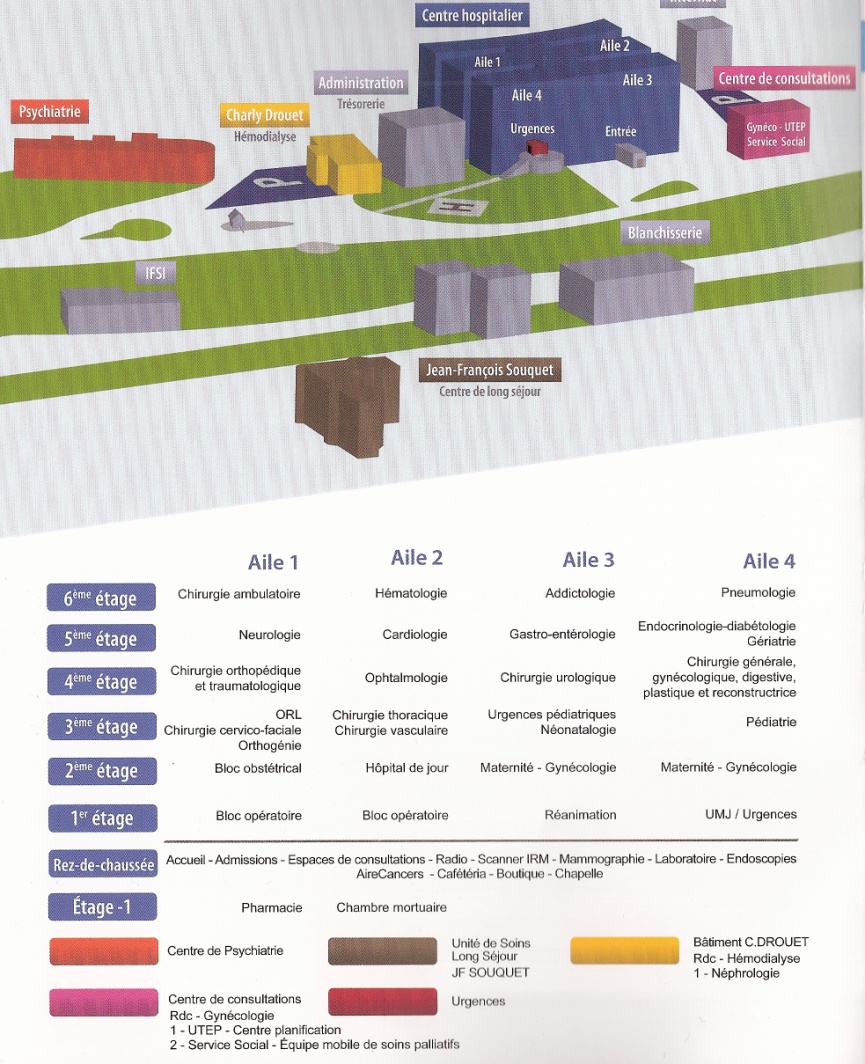
pour la mise en place, selon la norme et les
constructeurs, au sein du Centre Hospitalier de Boulogne
sur Mer. Mots clés : Norme -
Sécurité électrique - Test - Essai
- Électromédical |
||
|
This course has been
essentially undertaken for patient and staff security
purpose by introducing the new international standard
based on medical electrical equipment trials : CEI 62353
dated on 2007. In this report, you will
find explanations about specifications of this norm and
advice to apply this standard within the Boulogne
Hospital. Key words : Standard - Electric Security - Trial
- Electromedical |
||




 et
et 
 et
et 
 et
et